иҝҮж•ҸжҖ§з–ҫз—…йҷӨдәҶе…Қз–«з»ҶиғһиҝҳиғҪз ”з©¶д»Җд№ҲпјҹиҝҷзҜҮScienceеӯҗеҲҠзҡ„зӢ¬зү№жҖқи·ҜеҖјеҫ—еҖҹйүҙ
ж’°еҶҷпјҡе…«еҚҰе°ҸеёҲеҰ№ жқҘжәҗпјҡе°Ҹеј иҒҠз§‘з ”е№іеҸ°зҡ„“ иҜҫйўҳжҢҮеҚ—й’Ҳ”е…¬дј—еҸ·пјҢеҫ®дҝЎе…¬дј—еҸ·жҗңзҙў“ иҜҫйўҳжҢҮеҚ—й’Ҳ”еҚіеҸҜе…іжіЁ/жү«жҸҸе…іжіЁи§Ғж–Үжң«
#еӣҪиҮӘ然# #з§‘з ”зғӯзӮ№# #иҜҫйўҳжҖқи·Ҝ#
иҝҮж•ҸжҖ§з–ҫз—…жҳҜеҪұе“Қдәәзұ»зҡ„жңҖжҷ®йҒҚз–ҫз—…д№ӢдёҖпјҢе…¶жӮЈз—…зҺҮжӯЈд»Ҙжҳҫи‘—зҡ„йҖҹеәҰдёҠеҚҮгҖӮд»ҠеӨ©иҰҒз»ҷеӨ§е®¶еёҰжқҘзҡ„ж–Үз« жҳҜиҝ‘жңҹеҸ‘иЎЁеңЁScience Immunology(IF 30.630)дёҠзҡ„“Epithelial-intrinsic defects in TGFR signaling drive local allergic inflammation manifesting as eosinophilic esophagitis”пјҢж–Үз« дё»иҰҒи®Іиҝ°дәҶTGFβ еңЁжҺ§еҲ¶з»„з»Үзү№ејӮжҖ§иҝҮж•ҸжҖ§зӮҺз—Үж–№йқўиө·зқҖдёҖз§Қеҹәжң¬зҡ„гҖҒйқһеҶ—дҪҷзҡ„гҖҒдёҠзҡ®з»ҶиғһеҶ…еңЁзҡ„дҪңз”ЁпјҢиҝҷз§ҚдҪңз”ЁзӢ¬з«ӢдәҺе®ғеңЁйҖӮеә”жҖ§е…Қз–«дёӯзҡ„дҪңз”ЁгҖӮ

е—ңй…ёжҖ§зІ’з»ҶиғһжҖ§йЈҹз®ЎзӮҺ (EoE) жҳҜдёҖз§Қд»ҘйЈҹз®Ўе—ңй…ёжҖ§зІ’з»ҶиғһжҖ§зӮҺз—Үдёәзү№еҫҒзҡ„ж…ўжҖ§з–ҫз—…пјҢжӮЈиҖ…йҖҡеёёиЎЁзҺ°дёәеҗһе’Ҫеӣ°йҡҫе’ҢйЈҹзү©еөҢеЎһгҖӮEoE дёҺе…¶д»–иҝҮж•ҸжҖ§з–ҫз—…жңүи®ёеӨҡе…ұеҗҢзү№еҫҒпјҢеҢ…жӢ¬зӮҺжҖ§з»Ҷиғһжөёж¶Ұзҡ„зү№еҫҒгҖҒдёҠзҡ®еўһз”ҹзҡ„еӯҳеңЁд»ҘеҸҠдёҠзҡ®иЎҚз”ҹзҡ„иӯҰжҠҘзҙ зҡ„иҜұеҜјпјҢиЎЁжҳҺе…·жңүе…ұеҗҢзҡ„з—…зҗҶз”ҹзҗҶеӯҰзү№жҖ§гҖӮзҺҜеўғе’ҢйҒ—дј еӣ зҙ йғҪжңүеҸҜиғҪиҜұеҸ‘ EoEгҖӮеңЁдёҺ EoE зӣёе…ізҡ„еүҚ 10 дёӘеҹәеӣ еҸҳејӮдёӯпјҢеҮ д№ҺжүҖжңүеҸҳејӮйғҪеҸ‘з”ҹеңЁдёҠзҡ®з»ҶиғһиЎЁиҫҫзҡ„еҹәеӣ дёӯпјҢ并且еӨ§зәҰдёүеҲҶд№ӢдёҖзј–з ҒеҸӮдёҺиҪ¬еҢ–з”ҹй•ҝеӣ еӯҗ-β (TGFβ) дҝЎеҸ·иҪ¬еҜјзҡ„иӣӢзҷҪиҙЁгҖӮ
дҪңиҖ…еҸ‘зҺ°пјҢ R1 (Tgfbr1M318R) е°Ҹйј иғҪиҮӘеҸ‘еҸ‘еұ•еҮә EoEпјҢиҜҘ EoE е…·жңү 100% зҡ„еӨ–жҳҫзҺҮдё”дёҺдәәзұ»зҡ„з–ҫз—…зү№еҫҒйқһеёёжҺҘиҝ‘пјҢ并иҜҒжҳҺдёҠзҡ®еҸ‘иӮІдёӯзҡ„еҺҹеҸ‘жҖ§зјәйҷ·(зӢ¬з«ӢдәҺж·Ӣе·ҙз»ҶиғһжҲ–иҝҮж•ҸеҺҹ)еҸҜд»ҘеҗҜеҠЁ T иҫ…еҠ©з»Ҷиғһ 2 (TH2) зӮҺз—Үзә§иҒ”еҸҚеә”гҖӮйЈҹз®ЎдёҠзҡ®з»Ҷиғһдёӯ TGFβR дҝЎеҸ·еҮҸе°‘еҜјиҮҙз»Ҷиғһз”ҹй•ҝжҠ‘еҲ¶еҲҶеҢ–зЁӢеәҸж— ж•ҲпјҢ并еҜјиҮҙдҝғзӮҺд»ӢиҙЁиҝҮеәҰеўһж®–е’ҢеҲҶжіҢгҖӮдәҺжҳҜдҪңиҖ…жҸҗеҮәдәҶпјҢиҝҮж•ҸжҖ§з–ҫз—…зҡ„иө·жәҗжҳҜз”ұдёҠзҡ®з»Ҷиғһеј•еҸ‘зҡ„еұҖйғЁж— иҸҢжҖ§зӮҺз—ҮпјҢе°ҶдёҠзҡ®зҡ„дҪңз”Ёжү©еұ•еҲ°еұҸйҡңеҠҹиғҪд№ӢеӨ–пјҢе°Ҷе…¶е…ҲеӨ©е…Қз–«еҠҹиғҪеҢ…жӢ¬еңЁиҝҮж•ҸжҖ§з–ҫз—…дҪ“иҙЁдёӯгҖӮиҝҷдәӣеҸ‘зҺ°дҝғиҝӣдәҶдҪңиҖ…еҜ№еёёи§„йҷҗеҲ¶з»„з»Үзү№ејӮжҖ§иҝҮж•ҸжҖ§зӮҺз—ҮжңәеҲ¶зҡ„зҗҶи§ЈгҖӮ
з ”з©¶з»“жһң
1. R1 е°Ҹйј иҮӘеҸ‘еҸ‘еұ•еҮәз¬ҰеҗҲ EoE иҜҠж–ӯж ҮеҮҶзҡ„з–ҫз—…
EoE жӮЈиҖ…жңҖеёёи§Ғзҡ„з—ҮзҠ¶жҳҜеҗһе’Ҫеӣ°йҡҫе’ҢйЈҹзү©еөҢеЎһгҖӮWT е°Ҹйј зҡ„йЈҹз®Ў(еӣҫ 1A)зӢӯзӘ„дё”йҖҡз•…пјҢиҖҢ R1 е°Ҹйј зҡ„йЈҹз®Ўжү©еӨ§(еӣҫ 1B)пјҢдёҺ WT е°Ҹйј зӣёжҜ”пјҢеҜ№R1 е°Ҹйј еҶІжҙ—йЈҹз®ЎеҗҺеӣһ收дәҶжӣҙеӨҡзҡ„еӣәдҪ“зү©иҙЁ(еӣҫ 1C). еңЁ R1 е°Ҹйј зҡ„йЈҹз®Ўз»„з»ҮжЁӘжҲӘйқўдёӯпјҢжү©еј е’ҢйЈҹзү©йҳ»еЎһд№ҹеҫҲжҳҺжҳҫ(еӣҫ 1D еҲ° 1G)гҖӮ
еӣ жӯӨпјҢR1 е°Ҹйј йЈҹз®Ўзҡ„дёҙеәҠе’Ңз»„з»ҮеӯҰзү№еҫҒж»Ўи¶іж—ўе®ҡзҡ„ EoE иҜҠж–ӯж ҮеҮҶгҖӮ
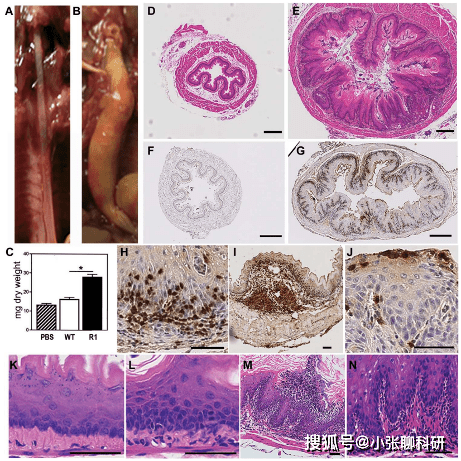
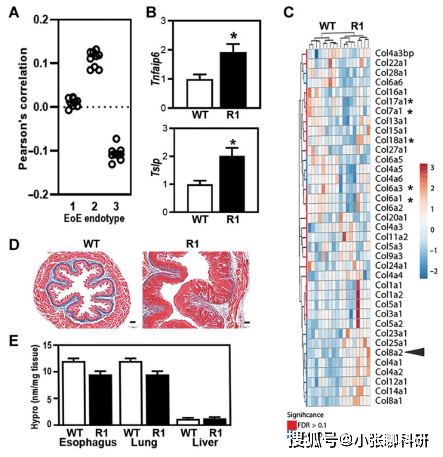
дёәдәҶзЎ®е®ҡ R1 е°Ҹйј е’Ңдәәзұ»з–ҫз—…еҶ…еһӢд№Ӣй—ҙзҡ„зӣёдјјзЁӢеәҰпјҢдҪңиҖ…еҜ№ R1 е°Ҹйј еҶ…йғЁйЈҹз®Ўз»„з»ҮиҝӣиЎҢдәҶ RNA жөӢеәҸ (RNA-seq)пјҢ并计算дәҶе°Ҹйј ж ·жң¬дёӯеҹәеӣ иЎЁиҫҫж°ҙе№ігҖӮ
еҢәеҲҶеҶ…еһӢзҡ„дёҖдёӘзү©зҗҶзү№еҫҒжҳҜ EoEe2 дёӯжІЎжңүзәӨз»ҙеҢ–пјҢиҖҢ EoEe3 дёӯеӯҳеңЁзәӨз»ҙзӢӯзӘ„гҖӮR1 е°Ҹйј жІЎжңүзӢӯзӘ„зҡ„йЈҹйҒ“пјҢ并且 R1 дёӯиЎЁиҫҫжңҖй«ҳзҡ„иғ¶еҺҹиӣӢзҷҪеҹәеӣ дҪҺдәҺ WT йЈҹйҒ“гҖӮиҝҷдәӣзҰ»дҪ“ж•°жҚ®дёҺдҪ“еӨ–ж•°жҚ®дёҖиҮҙпјҢдҪ“еӨ–ж•°жҚ®иЎЁжҳҺеңЁиҪ¬жҹ“ Tgfbr1M318R зҡ„з»ҶиғһдёӯпјҢSMAD йқ¶еҹәеӣ зҡ„иҜұеҜјеҸ—жҚҹгҖӮ
然еҗҺдҪңиҖ…е°Ҷеҹәеӣ иЎЁиҫҫеҲҶжһҗжү©еұ•еҲ° EoE иҜҠж–ӯеҹәеӣ з»„д№ӢеӨ–гҖӮзұ»дјјдәҺдәәзұ»жҙ»жЈҖз”ҹжҲҗзҡ„ж•°жҚ®йӣҶпјҢеӨ§еӨҡж•°зҡ„е·®ејӮиЎЁиҫҫеҹәеӣ еңЁ R1 дёӯй«ҳдәҺ WT йЈҹз®ЎгҖӮдёҺжңҖиҝ‘зҡ„жөҒејҸз»ҶиғһжңҜе’ҢжқҘиҮӘдәәдҪ“з»„з»Үжҙ»жЈҖзҡ„еҚ•з»Ҷиғһеҹәеӣ иЎЁиҫҫж•°жҚ®дёҖиҮҙпјҢWT е’Ң R1 йЈҹз®Ўдёӯзҡ„ B з»ҶиғһгҖҒе—ңзўұжҖ§зІ’з»ҶиғһгҖҒзІ’з»Ҷиғһе’ҢиҮӘ然жқҖдјӨз»Ҷиғһж•°йҮҸеҫҲе°‘гҖӮ
жҖ»д№ӢпјҢTGFβR дҝЎеҸ·зјәйҷ·е°Ҹйј зҡ„еҸ‘з—…е№ҙйҫ„гҖҒиҪ¬еҪ•з»„гҖҒдёҙеәҠзү№еҫҒгҖҒз»„з»ҮеӯҰзү№еҫҒе’ҢзӮҺз—Үжөёж¶Ұе…ұеҗҢжҰӮжӢ¬дәҶдәәзұ» EoEe2 зҡ„з–ҫз—…зү№еҫҒгҖӮ
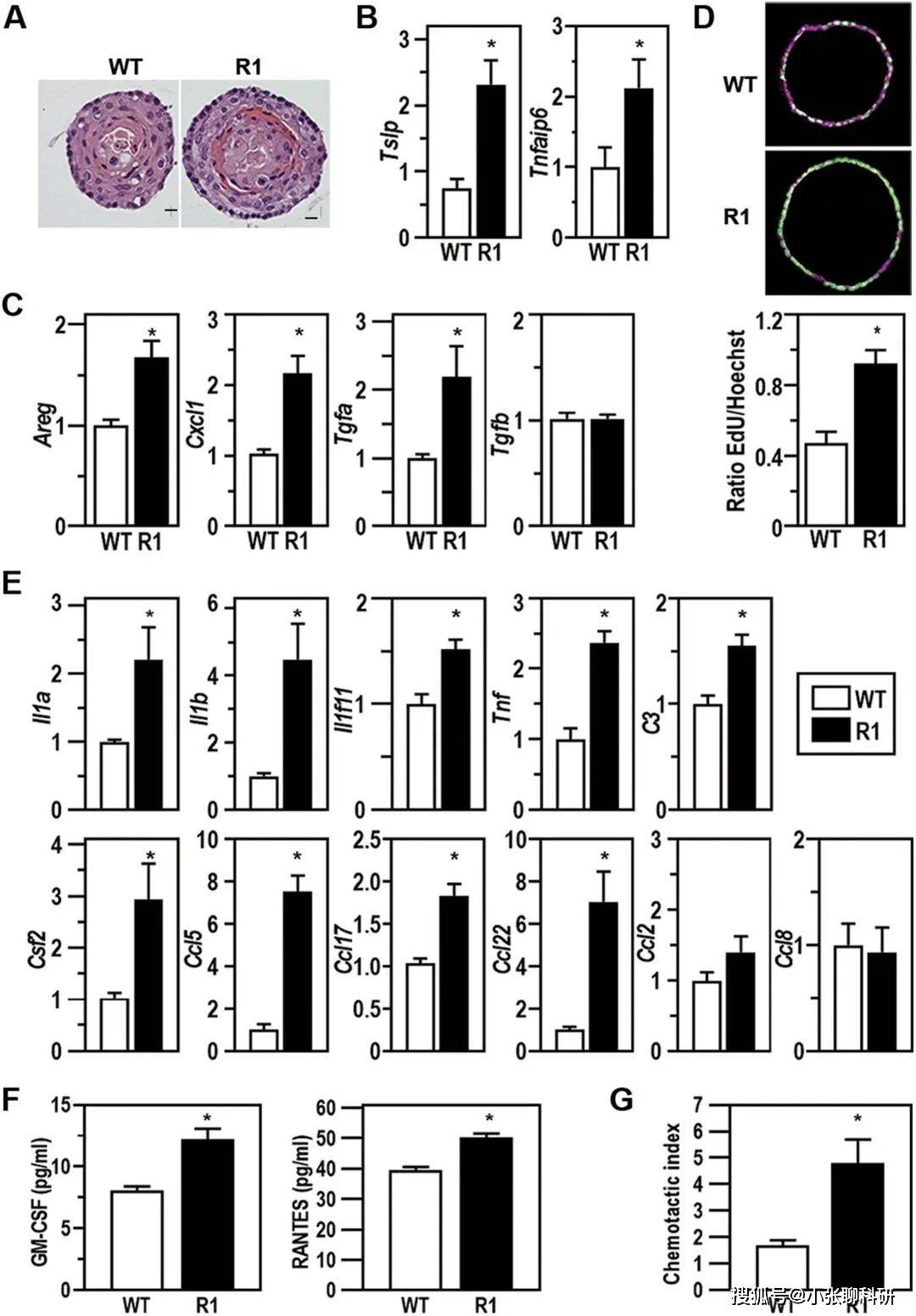
дёәдәҶзЎ®е®ҡ T з»ҶиғһеҰӮдҪ•еҪұе“Қ R1 е°Ҹйј зҡ„ EoE з—…зҗҶеӯҰпјҢдҪңиҖ…е°Ҷ R1 еҸҳдҪ“еј•е…Ҙе…ҲеӨ©жҖ§зјәд№Ҹж·Ӣе·ҙз»Ҷиғһзҡ„е°Ҹйј дёӯгҖӮе®һйӘҢеҫ—еҮәзҡ„з»“и®әжҳҜз”ұ R1 еҸҳдҪ“еј•иө·зҡ„ EoE иЎЁеһӢзҡ„д»»дҪ•ж–№йқўйғҪдёҚжҳҜж·Ӣе·ҙз»Ҷиғһдҫқиө–жҖ§зҡ„(еӣҫ3H-O)гҖӮ

дёәдәҶиҜ„дј°йӘЁй«“ (BM) иЎҚз”ҹз»ҶиғһдёҺйқһйҖ иЎҖз»Ҷиғһдёӯ TGFβR дҝЎеҸ·ж”№еҸҳеҜ№ EoE з—…зҗҶз”ҹзҗҶеӯҰзҡ„зӣёеҜ№еҪұе“ҚпјҢдҪңиҖ…еҜ№ R1 е°Ҹйј иҝӣиЎҢдәҶиҫҗ照并用 WT BM йҮҚе»әгҖӮйҮҚе»әе…«е‘ЁеҗҺпјҢWT дҫӣдҪ“ BM иЎҚз”ҹзҡ„е—ңй…ёжҖ§зІ’з»ҶиғһеңЁ R1 е°Ҹйј зҡ„йЈҹйҒ“дёӯз§ҜзҙҜ(еӣҫ 4A)пјҢ并дјҙжңүйЈҹйҒ“жү©еј е’ҢйЈҹзү©еөҢеЎһ(еӣҫ 4B)гҖӮ
еӣ жӯӨпјҢж”ҫе°„жҠөжҠ—зҡ„е®ҝдё»з»ҶиғһдёӯеҮҸејұзҡ„ TGFβR1 дҝЎеҸ·дј еҜјеҜ№дәҺеңЁ R1 е°Ҹйј дёӯеј•иө· EoE жҳҜеҝ…иҰҒдё”е……еҲҶзҡ„гҖӮзӣёеҸҚпјҢд»… BM иЎҚз”ҹз»Ҷиғһдёӯж”№еҸҳзҡ„ TGFβR1 дҝЎеҸ·дёҚдјҡеј•иө·з–ҫз—…гҖӮ
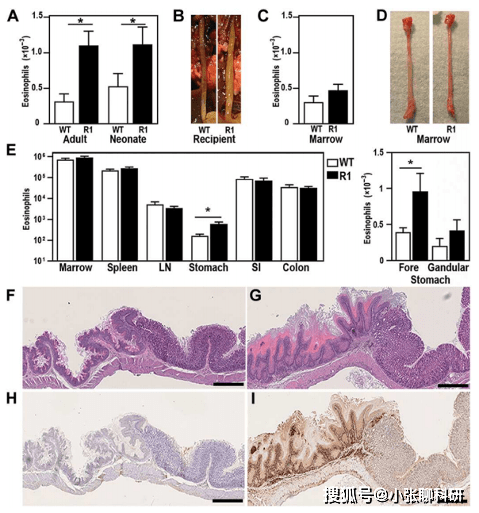
EoE зҡ„иҜҠж–ӯж ҮеҮҶжҳҜе—ңй…ёжҖ§зІ’з»ҶиғһзӮҺз—ҮдёҺйЈҹйҒ“еҲҶзҰ»гҖӮжңүз ”з©¶и°ғжҹҘиҜҒе®һпјҢе—ңй…ёжҖ§зІ’з»ҶиғһеңЁ R1 е°Ҹйј зҡ„ BMгҖҒж·Ӣе·ҙеҷЁе®ҳжҲ–иӮ йҒ“дёӯжІЎжңүеўһеҠ (еӣҫ 4E)гҖӮR1 е°Ҹйј зҡ„еүҚиғғд№ҹиЎЁзҺ°еҮәдёҺйЈҹз®ЎзӣёеҗҢзҡ„з»„з»Үз—…зҗҶеӯҰзү№еҫҒгҖӮдҪңиҖ…и§ӮеҜҹеҲ°е—ңй…ёжҖ§зІ’з»ҶиғһеңЁ R1 е°Ҹйј дёӯзҡ„з§ҜзҙҜеңЁи§Јеү–еӯҰдёҠд»…йҷҗдәҺз”ұеӨҚеұӮйіһзҠ¶дёҠзҡ®жҺ’еҲ—зҡ„з»„з»ҮпјҢиҝҷиЎЁжҳҺдәҶиҝҷдәӣзү№еҢ–з»ҶиғһжҳҜз»„з»ҮйҷҗеҲ¶жҖ§зӮҺз—Үзҡ„еҺҹеӣ гҖӮ
6. R1 е°Ҹйј зҡ„ EoE дёҚжҳҜеҹәдәҺж”№еҸҳзҡ„йЈҹз®ЎеұҸйҡңеҠҹиғҪ
дҪңиҖ…иҜ•еӣҫдәҶи§ЈдёҠзҡ®з»Ҷиғһй©ұеҠЁиҝҮж•ҸжҖ§зӮҺз—Үзҡ„жңәеҲ¶гҖӮеңЁеҒҘеә·еҲҶеҢ–зҡ„и§’иҙЁеҪўжҲҗз»ҶиғһдёӯпјҢзј–з ҒеӨ–зҡ®иӣӢзҷҪ (IVL)гҖҒenvoplakin (EVPL) е’Ң periplakin (PPL) зҡ„еҹәеӣ иў«еҗҢж—¶иҜұеҜјпјҢ然еҗҺжҳҜиҒҡдёқиӣӢзҷҪ (FLG) е’Ңе…ңз”ІиӣӢзҷҪ (LOR)пјҢд»ҘеҸҠжЎҘзІ’ж ёеҝғиӣӢзҷҪ 1 (DSG1)гҖӮ
дёәдәҶзЎ®е®ҡи§ӮеҜҹеҲ°зҡ„еҹәеӣ иЎЁиҫҫеҸҳеҢ–жҳҜеҗҰеҪұе“Қз»Ҷиғһй—ҙжҺҘи§ҰпјҢдҪңиҖ…дҪҝз”ЁйҖҸе°„з”өеӯҗжҳҫеҫ®й•ңжЈҖжҹҘдәҶйЈҹз®ЎдёҠзҡ®зҡ„з»“жһ„гҖӮйў—зІ’еұӮеҢ…еҗ«жүҒе№ігҖҒзҙ§еҜҶе Ҷз§Ҝзҡ„з»ҶиғһпјҢиҝҷдәӣз»ҶиғһйҖҡиҝҮжҜҸдёӘз»Ҷиғһе‘Ёиҫ№еқҮеҢҖеҲҶеёғзҡ„жЎҘзІ’зӣёдә’иҝһжҺҘгҖӮжЈҳеұӮеҢ…еҗ«жңүж ёз»ҶиғһпјҢд»Һз«Ӣж–№дҪ“иҪ¬еҸҳдёәжүҒе№ідҪ“пјҢ并йҖҡиҝҮеӨҡеҲәзӘҒиө·д№Ӣй—ҙзҡ„жЎҘзІ’зӣёдә’иҝһжҺҘгҖӮеңЁеҹәеә•дёҠеұӮдёӯж—ўжІЎжңүи§ӮеҜҹеҲ°жү©еј зҡ„з»Ҷиғһй—ҙйҡҷ (ICS)пјҢд№ҹжІЎжңүи§ӮеҜҹеҲ°жЎҘзІ’зҡ„ж•°йҮҸгҖҒеҲҶеёғжҲ–з»“жһ„зҡ„еҸҳеҢ–гҖӮ
дёҺеҹәеә•еұӮзӣёжҜ”пјҢR1 е’Ң WT йЈҹз®Ўд№Ӣй—ҙзҡ„е®һиҙЁжҖ§е·®ејӮеӯҳеңЁдәҺеҹәеә•еұӮдёӯгҖӮиҖҢиҝҷдёҖеұӮд»…з”ұ WT йЈҹз®Ўдёӯзҡ„дёҖдёӘжҲ–дёӨдёӘз«Ӣж–№еҪўз»Ҷиғһз»„жҲҗ(еӣҫ 5K)гҖӮдёәдәҶзЎ®е®ҡ R1 е°Ҹйј еҹәеӣ иЎЁиҫҫе’Ңи¶…еҫ®з»“жһ„зү№еҫҒзҡ„е·®ејӮжҳҜеҗҰеҜјиҮҙйЈҹз®ЎеұҸйҡңжё—жјҸпјҢдҪңиҖ…иҜ„дј°дәҶеұҸйҡңеҠҹиғҪгҖӮи·ЁдёҠзҡ®з”өйҳ» (TEER) з”ЁдәҺе®ҡйҮҸйЈҹз®Ўз»„з»Үзҡ„з”өйҳ»жҠ—(еӣҫ 5R)гҖӮ
еҫ—еҮәзҡ„з»“и®әжҳҜпјҢйЈҹз®ЎеұҸйҡңеҠҹиғҪзҡ„з ҙеқҸж— жі•и§ЈйҮҠ R1 е°Ҹйј дёӯ EoE зҡ„еҸ‘еұ•гҖӮ
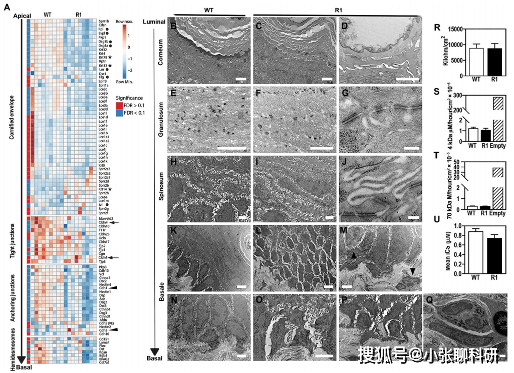
з”ұдәҺйЈҹз®ЎеұҸйҡңеҠҹиғҪе®ҢеҘҪж— жҚҹпјҢдҪңиҖ…дёӢдёҖжӯҘжҳҜзЎ®е®ҡе“Әдәӣе…¶д»–жңәеҲ¶еҸҜиғҪеҜјиҮҙ R1 йЈҹз®ЎеҸ‘зӮҺгҖӮдёҺ WT йЈҹз®ЎзӣёжҜ”пјҢR1 дёӯ Cdh3 зҡ„иЎЁиҫҫжӣҙй«ҳпјҢCdh1 зҡ„иЎЁиҫҫжӣҙдҪҺ(еӣҫ 5AпјҢв—„)гҖӮCdh1гҖҒCdh3 е’Ң Cldn1 зҡ„еҗҜеҠЁеӯҗдёҚеҢ…еҗ«е…ёеһӢзҡ„ SMAD з»“еҗҲеҹәеәҸпјҢиЎЁжҳҺе®ғ们еңЁ R1 дёҠзҡ®з»Ҷиғһдёӯзҡ„еӨұи°ғжҳҜй—ҙжҺҘзҡ„гҖӮ
и§’иӣӢзҷҪеҹәеӣ еңЁеҸ‘иӮІиҝҮзЁӢдёӯеҸ—еҲ°дёҘж ји°ғжҺ§пјҢеҸҜз”ЁдәҺиҜ„дј°и§’иҙЁеҪўжҲҗз»ҶиғһеҲҶеҢ–гҖӮжӯЈеҰӮйў„жңҹзҡ„йӮЈж ·пјҢWT йЈҹз®Ўдёӯзҡ„ K14 (и§’иӣӢзҷҪ14)д»…йҷҗдәҺдёҖеұӮи–„и–„зҡ„еҹәеә•з»ҶиғһгҖӮ
дҪңиҖ…继з»ӯжҜ”иҫғеҲҶеҢ–е’Ңеҹәеә•и§’иҙЁеҪўжҲҗз»Ҷиғһд№Ӣй—ҙиЎЁиҫҫе·®ејӮжңҖеӨ§еҹәеӣ зҡ„иЎЁиҫҫйҮҸпјҢR1 йЈҹз®Ўзҡ„иҪ¬еҪ•з»„иЎЁжҳҺеӯҳеңЁејӮеёёзҡ„з»Ҷиғһе‘Ёжңҹи°ғиҠӮгҖӮ
иҝҷдәӣж•°жҚ®иЎЁжҳҺпјҢйіһзҠ¶дёҠзҡ®з»Ҷиғһдёӯ TGFβR дҝЎеҸ·дј еҜјзҡ„еҮҸе°‘дјҡжҚҹе®із»Ҷиғһе‘Ёжңҹи°ғиҠӮпјҢиЎЁзҺ°дёәеҹәеә•з»Ҷиғһеўһз”ҹпјҢиҝҷжҳҜ EoE дёҖдёӘжҳҫи‘—зҡ„з»„з»ҮеӯҰзү№еҫҒгҖӮ
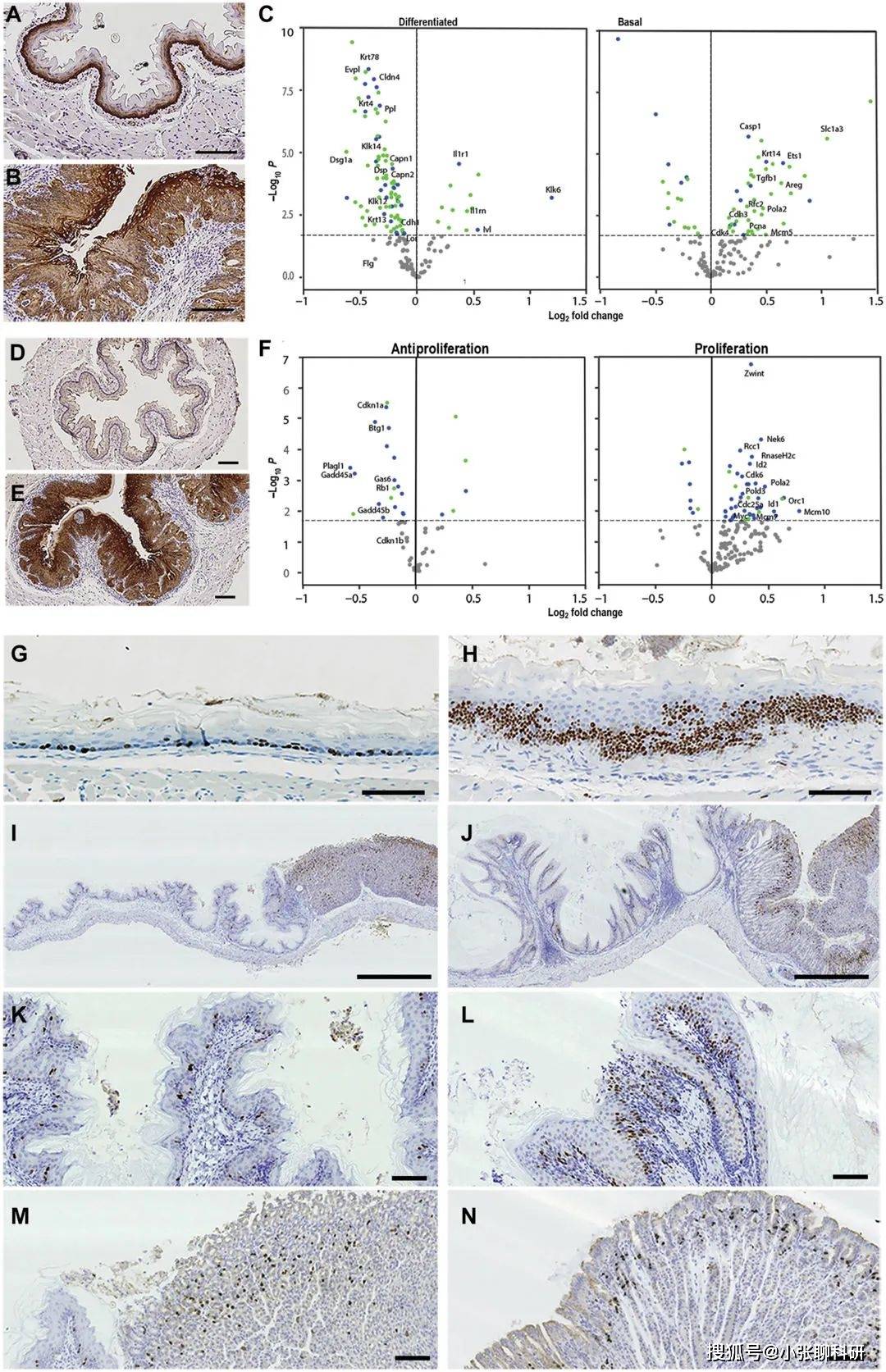
жҖ»зҡ„жқҘиҜҙпјҢдҪңиҖ…зҡ„з ”з©¶з»“жһңиЎЁжҳҺ R1 йЈҹз®ЎдёӯжңӘжҲҗзҶҹгҖҒиҝҮеәҰеўһж®–е’ҢеҸ—жҚҹзҡ„дёҠзҡ®з»Ҷиғһз§ҜзҙҜгҖӮдҪңиҖ…иҜ•еӣҫзЎ®е®ҡиҝҷдәӣ TGFβ иҜұеҜјзҡ„дёҠзҡ®з»ҶиғһзЁіжҖҒжү°еҠЁеҸҜиғҪеҜјиҮҙзӮҺз—Үзҡ„жңәеҲ¶гҖӮз»“жһңжҳҫзӨәR1 йЈҹз®Ўе…·жңү IL-1 е’Ң TNFα ж…ўжҖ§жҝҖжҙ»зҡ„зӮҺз—Үзү№еҫҒ(еӣҫ 7A е’ҢиЎЁ S6 е’Ң S7)гҖӮеұҸйҡңиЎЁйқўзҡ„зӮҺз—Үзә§иҒ”еҸҚеә”еҸҜиғҪз”ЁдәҺйҳІжӯўж„ҹжҹ“еӣ еӯҗ并дҝғиҝӣдјӨеҸЈж„ҲеҗҲгҖӮ
дҪңиҖ…йҖүжӢ©дәҶеҮ з§Қе…·жңүиҝҮж•ҸжҖ§зӮҺз—Үе’ҢдёҠзҡ®иҝҮеәҰеўһж®–зү№еҫҒзҡ„еҲҶеӯҗпјҢз”ЁдәҺеңЁиӣӢзҷҪиҙЁе’Ңи§Јеү–еӯҰж°ҙе№ідёҠиҝӣиЎҢиҝӣдёҖжӯҘз ”з©¶(еӣҫ 7B иҮі 7IпјҢд»ҘеҸҠеӣҫ S7)пјҢиЎЁжҳҺиҝҷдәӣзү№еҢ–дёҠзҡ®з»Ҷиғһдёӯ TGFβR дҝЎеҸ·еҮҸејұжҳҜеҜјиҮҙ R1 е°Ҹйј з»„з»ҮйҷҗеҲ¶жҖ§е—ңй…ёжҖ§зІ’з»ҶиғһзӮҺз—Үзҡ„еҺҹеӣ гҖӮеӣ жӯӨпјҢе°Ҫз®Ў R1 е°Ҹйј зҡ„йЈҹз®ЎдёҠзҡ®з»“жһ„е®Ңж•ҙпјҢдҪҶ TGFβR дҝЎеҸ·зҡ„еҮҸе°‘еҜјиҮҙйіһзҠ¶дёҠзҡ®з»Ҷиғһзҡ„е…Қз–«з»ҶиғһеҠҹиғҪжҝҖжҙ»е’Ңж”№еҸҳгҖӮ
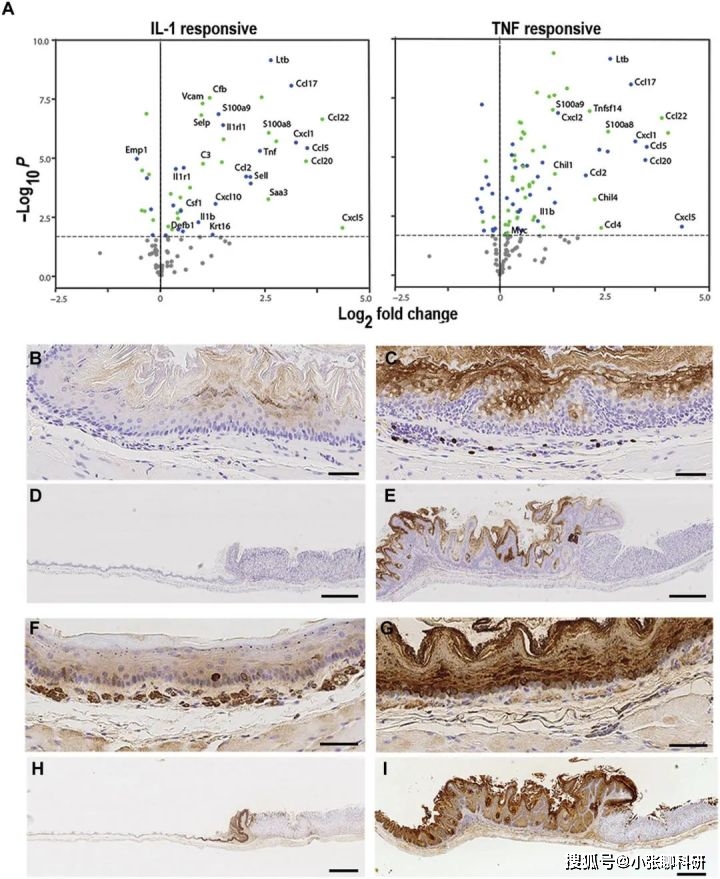
йіһзҠ¶дёҠзҡ®з»Ҷиғһдёӯ TGFβR дҝЎеҸ·дј еҜјзҡ„еҮҸе°‘жҳҜ EoE еҸ‘з—…жңәеҲ¶зҡ„ж ёеҝғгҖӮ然иҖҢпјҢзҰ»дҪ“йЈҹз®Ўз»„з»Үдёӯзҡ„еҹәеӣ иЎЁиҫҫеҸҳеҢ–еҸҚжҳ дәҶи®ёеӨҡз»Ҷиғһзұ»еһӢдёӯ TGFβR дҝЎеҸ·иҪ¬еҜјж”№еҸҳзҡ„жҖ»е’ҢгҖӮиҷҪ然дёҚжҳҜз»қеҜ№йңҖиҰҒпјҢдҪҶйқһдёҠзҡ®е…ҲеӨ©з»Ҷиғһд№ҹеҸҜиғҪеңЁдҪ“еҶ…дҝғжҲҗ EoE з—…зҗҶеӯҰгҖӮ
жҖ»з»“
жҖ»зҡ„жқҘиҜҙпјҢдҪңиҖ…зҡ„з ”з©¶з»“жһңе°ҶдёҠзҡ®з»ҶиғһдҪңдёәиҝҮж•Ҹзү№еҫҒзҡ„еҹәзҹіпјҢ并жү©еӨ§дәҶ TGFβ еңЁз»ҙжҢҒе…Қз–«зЁіжҖҒж–№йқўзҡ„еӨҡз»ҙдҪңз”ЁгҖӮжң¬ж–Үз ”з©¶зҡ„дёҖдёӘеұҖйҷҗжҖ§жҳҜдҪңиҖ…еҸӘе…іжіЁдёҠзҡ®з»ҶиғһдҪңдёә еҶіе®ҡEoE зҡ„з»Ҷиғһзұ»еһӢпјҢ йңҖиҰҒиҝӣдёҖжӯҘзҡ„з ”з©¶жқҘзЎ®е®ҡе…¶д»–еҹәиҙЁз»Ҷиғһе’Ң/жҲ–йҖ иЎҖз»Ҷиғһи°ұзі»жҳҜеҗҰжҲ–еҰӮдҪ•дҝғиҝӣ EoEгҖӮиҝҳйңҖиҰҒиҝӣдёҖжӯҘзҡ„з ”з©¶жқҘдәҶи§Јеҫ®з”ҹзү©з»„е’ҢйҘ®йЈҹзӯүеӨ–йғЁеӣ зҙ еҰӮдҪ•еҪұе“ҚйЈҹз®ЎдёҠзҡ®зЁіжҖҒгҖӮдҪңиҖ…йў„и®ЎйЈҹз®Ўе—ңй…ёжҖ§зІ’з»ҶиғһзӮҺз—ҮжҪңеңЁзҡ„з—…еӣ жңәеҲ¶д№ҹдёҺеҸ‘з”ҹеңЁзү№ж®ҠдёҠзҡ®з»„з»ҮеҶ…зҡ„е…¶д»–иҝҮж•ҸжҖ§з–ҫз—…й«ҳеәҰзӣёе…іпјҢеҢ…жӢ¬зү№еә”жҖ§зҡ®зӮҺгҖҒйЈҹзү©иҝҮж•Ҹе’ҢеӯЈиҠӮжҖ§иҝҮж•ҸгҖӮ
еҺҹж–Үй“ҫжҺҘпјҡhttps://mp.weixin.qq.com/s/xg29mT5bTT7A8g2WJg_juw











